? ? ? ?來源:閑談 Immunology ? ? ? ?在進行生物信息學評估之后,通常會通過全面產品表征,對潛在候選分子進行實驗評估。 ? ? ? ?與mAb成藥性評估高度相關的質量屬性,匯總在下表中。 ? ? ? ?通常,用于可開發性評估的樣本,是通過瞬時轉染(例如HEK293細胞)產生的。可以評估與表達宿主無關的特性,例如一級序列,疏水性,溶解性,熱穩定性和抗原結合親和力。 ? ? ? ?因為PTM高度依賴于細胞系和細胞培養條件,因此通過可開發性評估,候選分子進入工藝開發階段,通常換成CHO等細胞,穩定表達,進行工藝優化。 ? ? ? ?1. 一級結構確認和序列變異體 ? ? ? ?預期氨基酸序列的構象是進一步分析和開發mAb先導候選分子的先決條件。現代質譜(MS)具有以≤2Da的精度準確測量IgG的分子量(約150kDa)的能力。可以通過液質聯用(LC-MS)和MS/MS肽圖確認完整的一級序列。 多項研究表明存在低豐度序列變異體,通過使用LCMS/MS與數據庫搜索相結合,可以檢測和鑒定低水平的序列變異體;存在極低豐度序列變異體的原因:可能是自然發生的轉錄和翻譯過程中的低頻錯誤。 ? ? ? ?通過產品表征,可以選擇具有最小序列變異的mAb候選分子和克隆。 ? ? ? ?2. 翻譯后修飾 ? ? ? ?LC-MS具有很高的靈敏度,快速的周轉時間,最重要的是能夠獲得深入序列及修飾信息,因此在可開發性評估中起著至關重要的作用。可從LC-MS完整分析,從亞基或肽水平獲得PTM信息。 ? ? ? ?LC-MS分析能夠檢測各類修飾,例如糖型,N末端pyroGlu,C末端Lys,C末端酰胺化和糖基化。在亞基水平或還原成輕鏈和重鏈后的LC-MS分析將修飾定位于Fab,F(ab′)2,Fc區,輕鏈或重鏈。 ? ? ? ?除了傳統上使用的木瓜蛋白酶,使用有限的Lys-C或Ides酶消化可以實現更特異性的消化。IdeS消化和還原的結合,將每個片段的分子量降低到23-25 kDa,從而可以測量單同位素分子量。最終,在肽水平上的分析,可以精確定位完整和亞基水平的修飾位點。更重要的是,在肽水平上的分析,可以檢測到在完整和亞基水平上無法檢測到的修飾,例如Asn脫酰胺,分子量差異約為1 Da。由于色譜分離,沒有分子量差異的修飾,例如Asp異構化,從L-Cys到D-Cys和Ser外消旋化,也可以通過LC-MS檢測。 ? ? ? ?基于安全性和功效考慮修飾 ? ? ? ?修飾與安全性和功效問題有關。包括脫酰胺,異構化,Met和Trp氧化,未配對的半胱氨酸和可變域中的其他糖基化。在擴展的表征和強制降解研究期間,應仔細檢查這些修飾。 ? ? ? ?寡糖有三種類型,α1,3-Gal,NGNA和高甘露糖,應仔細評估。如前所述,α1,3-Gal和NGNA具有免疫原性。由于缺乏核心巖藻糖,高甘露糖已被證明可導致較短的體內半衰期并增強抗體依賴性細胞介導的細胞毒性(ADCC)。 ? ? ? ?此外,由于巖藻糖基化水平與增強的ADCC相關,因此必須對其進行監測,這取決于mAb的作用機理(MOA),可能是有益的或有害的。對于需要抗體依賴細胞殺傷靶細胞,則是有益的,但對于阻斷性抗體,則是有害的。 ? ? ? ?與降解相關的修飾 ? ? ? ?尚未報道這組修飾會影響產品的安全性或功效,但可能會引起免疫原性(因為這些修飾在人類內源性IgG或降解產物中均不存在),這組修飾包括部分前導序列,三硫鍵,硫醚和糖基化。為了最大程度地降低這種風險,應選擇這些修飾類型中含量最低的單克隆抗體候選物。此類別中的修飾也可能高度依賴于細胞系和細胞培養參數,例如溫度,pH,培養基組成和配方。 引起異質性的修飾 ? ? ? ?N末端pyroGlu的形成和C末端Lys的部分去除是引起異質性的兩個特征修飾,但對安全性或功效沒有影響。另外,這些修飾的水平高度依賴于細胞系和細胞培養條件。 與Fc的糖基化相關的末端Gal的水平也由于其對過程變化的敏感性而值得注意。末端Gal對結構,穩定性或清除沒有影響。最近的研究表明,末端半乳糖可能對ADCC的影響最小,但對CDC((complement dependent cytotoxicity test) 補體依賴的細胞毒性試驗)的影響卻很大。因此,對于涉及CDC的MOA的mAb候選分子,應考慮末端半乳糖的水平。由于末端半乳糖基化的水平隨細胞系和細胞培養條件的不同而變化,因此在開發過程的后期可能需要重新評估。 ? ? ? ?3. FcRn親和力 ? ? ? ?FcRn結合是影響mAb半衰期的最關鍵因素之一。通常通過Biacore測量mAb候選物的FcRn結合親和力,已開始使用生物層干涉術(BLI)或FcRn親和色譜的新替代方法。與Biacore和親和色譜相比,使用BLI可獲得更高的通量。通常,在酸性pH下具有更強FcRn結合,但在中性pH下具有快速解離的mAb,顯示出更長的體內半衰期。 ? ? ? ?4. 熱穩定性 ? ? ? ?熱穩定性是蛋白質在不同溫度環境下維持其結構和功能完整性的能力,并且是mAb的固有特性,可在制造和存儲過程中影響產品的穩定性,例如聚集。mAb候選物的高熱穩定性表明結構良好,需要更多的能量才能展開。因此,mAb的較高熱穩定性通常與較低的部分展開和聚集趨勢相關。除了聚集以外,還顯示出熱穩定性較低的單克隆抗體的表達也較低。 通常通過差示掃描量熱法(DSC)來測量熱穩定性。使用差示掃描熒光法(DSF)可以對96或384個樣品進行高通量熱穩定性篩選。可以基于獲得的熱力學參數(例如,展開的中點溫度(Tm)或展開溫度的起始時間(Tonset))對在相同條件下分析的多個候選對象進行排名。 ? ? ? ?5.溶解度 ? ? ? ?溶解度是mAb的重要可開發性參數,尤其是考慮到更高濃度制劑(100 mg / mL及更高濃度)發展的趨勢。單克隆抗體在整個加工,儲存和給藥過程中必須保持可溶。低溶解度會導致純化,無菌過濾,填充和精加工,運輸,儲存過程中出現問題,更重要的是,會影響活性,生物利用度和免疫原性。從方法來看,對于所有色譜步驟,在用于生物處理的緩沖液中的最小溶解度(例如20-30mg/mL)是必需的。在最終的超濾/滲濾(UF/DF)步驟中,將單克隆抗體以高于目標藥物產品的濃度緩沖液交換到制劑緩沖液中,因此需要更高的溶解度。 ? ? ? ?單抗較低的溶解度通常是由于與暴露的疏水或帶電斑塊的強烈自締合引起的。單克隆抗體的二價性質放大了它們的自締合趨勢。由構象變化或化學修飾引起的膠體不穩定性也會導致mAb的溶解性差。此外,mAb的溶解度通常受溶液性質的影響,例如緩沖液的組成,離子強度,pH和溫度。 ? ? ? ?根據氨基酸序列預測mAb候選物的溶解度具有挑戰性,因此應通過實驗研究mAb的溶解度。但是,研究mAb的溶解度直接需要大量的蛋白質,通常為數百毫克,因此通常不生產如此大量的所有候選物用于溶解度研究。由于可用于開發性評估研究的樣本數量有限,因此通常使用間接測量方法。例如,向mAb溶液中添加聚乙二醇(PEG)會導致濃度低得多的沉淀,因此可通過外推至PEG濃度為零來確定mAb的表觀溶解度。可以以高通量方式為mAb候選者選擇實現此方法。但是,PEG誘導的沉淀可能無法真正反映mAbs溶解度差的機理,因此應考慮采用正交方法或直接評估高濃度下的溶解度以確認預測的溶解度或驗證等級順序。 ? ? ? ?還可以通過測量滲透第二維里系數B22(與分子間相互作用相關的熱力學參數)來預測使用低濃度樣品的mAb的高濃度行為。正和負B22值分別表示排斥力或吸引力。影響B22的參數包括靜電相互作用,范德華力,排除體積,水合力和疏水作用。在許多獲得B22值的方法中,例如自相互作用色譜(SIC),膜滲透壓(MO)和分析超離心(AUC), 最常見的方法是通過靜態光散射(SLS)。最近,該值被用于確定通用溶解度線,即“液相線”,作為mAb相圖的一部分。 交叉相互作用色譜法(CIC)分析,由Jacob等人介紹。充分利用了色譜柱上的累積效應來捕獲測試mAb與大量(30mg)固定化人血清IgG之間的弱結合。由于暴露的粘性表面(疏水性或電荷性),CIC分析中洗脫較晚的單克隆抗體與溶解性差相關。另一個值得一提的方法是自相互作用納米粒子光譜學,它使用金納米粒子將mAb分子濃縮到高的局部濃度,以放大弱的自相互作用。該方法也可用于單克隆抗體候選物的高通量篩選。 ? ? ? ?6. 粘度 ? ? ? ?通過皮下(SC)注射給藥的高濃度藥物產品需要具有可控粘度的制劑,這使其成為早期評估的另一個關鍵因素,從而緩解可開發性問題。高粘度可能對最終的UF/DF步驟和填充/精加工操作構成挑戰。粘性藥品會導致輸送困難,導致患者依從性降低。粘性樣品還可能對分析方法的開發和儀器提出采樣挑戰。 ? ? ? ?mAb的高粘度是由于通過靜電或疏水相互作用或兩者結合而產生的強烈的自締合引起的。盡管可以探索許多配方參數,包括pH值,鹽,糖以及各種小分子賦形劑和去污劑,用以降低粘度。但是選擇最小內在問題,例如暴露于疏水性或帶電斑塊的mAb候選分子,是降低高粘度風險的最有效方法。 ? ? ? ?可以采用多種方法來測量粘度,包括Cannon-Fenske Routine粘度計,泰勒錐板法和各種流變儀。用于測量粘度的大多數常規技術需要大量材料。為了克服這一挑戰,特別是在可開發性評估方面,已開發出一種高通量DLS方法,該方法基于對高濃度mAb溶液中表觀聚苯乙烯珠半徑的測量,以反算mAb溶液的粘度。此方法僅可用于不與微珠相互作用的mAb,否則無法可靠地測量表觀微珠半徑。從DLS測量得出的高通量擴散相互作用參數也已顯示與粘度相關。近年來,允許使用≤100μL進行粘度測量并具有自動樣品處理功能的儀器已在市場上出售,它們適用于在開發性評估過程中測量粘度。 ? ? ? ?由于粘度對工藝和產品開發十分重要,因此,為開發性評估定義粘度目標是非常重要。制劑粘度至少應足夠低,以允許通過手動注射來遞送藥物制劑。粘度目標通常是根據每個公司的內部開發經驗制定的,尤其是在開發帶有預填充注射器和自動注射器裝置的SC產品時。例如,建議將粘度分為三類:1)“首選”粘度為10 cP或更低;2)10至20 cP之間的“可接受”粘度;和3)“不可接受”的粘度> 20 cP。可以將其用作定義粘度目標的起點,同時還要考慮工藝研發和產品開發的內部經驗以及輸送設備(例如自動注射器)的產品知識。 ? ? ? ?7.聚集傾向 ? ? ? ?聚集體是最常觀察到的與產品相關的雜質。由于其會導致免疫原性,所以需要進行密切監控。因此,它是可開發性評估的關鍵組成部分。除了使用預測工具外,還可以在擴展的表征和強制降解研究期間直接測量聚集傾向。盡管通常由于材料限制只能獲得低濃度的數據,但重要的是評估中高濃度(50-100 mg / mL)范圍內mAb的膠體穩定性和聚集傾向。 ? ? ? ?通常,十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳(SDS-PAGE)或毛細管電泳(CE-SDS)用于在變性條件下還原或非還原下測定mAb單體,片段和共價聚集體。多種方法可用于在天然條件下測量mAb可溶性聚集體(二聚體,低聚物或亞可見顆粒)。體積排阻色譜法(SEC)是確定mAb的高分子量蛋白(例如二聚體,三聚體或低聚物)和低分子量蛋白的最常用方法。它可以在擴展表征和強制降解期間評估聚集體。值得一提的是,SEC有時可以揭示單體,聚集體和碎片百分比以外的其他屬性。mAb的SEC異常行為(例如峰拖尾)可能表明其生物物理特性不理想。較長的保留時間和不對稱峰形可能表明mAb與SEC色譜柱之間存在非特異性相互作用。研究表明,SEC甚至可以將含有琥珀酰亞胺中間體的mAb變異體與具有Asn脫酰胺基(17Da)或Asp異構化(18Da)的單克隆抗體分離。SEC還顯示,包含氧化Trp的mAb變體早于主峰洗脫。這些示例表明,對SEC數據的解釋應謹慎進行,因為早晚的峰可能并不總是代表高分子量蛋白或者低分子量蛋白。 ? ? ? ?對于大型聚集體,可以使用光散射來表征<1nm至1-10μm范圍內的顆粒。DLS方法可用于確定mAb的流體動力學直徑和相互作用參數(例如KD),這些參數可在高通量模式下以較低的樣品消耗運行。也可以考慮使用測量濁度的方法(例如,可見波長處的光密度和濁度法)來檢測亞微米/亞可見顆粒。這些技術可以針對高通量和低的體積消耗來開發,因此可以用于可開發性評估。可以使用光阻法(例如HIAC)和流動成像方法(例如微流成像(MFI)進行亞可見粒子表征和定量,以檢測大于2μm的尺寸。目測方法用于檢測可見范圍內的蛋白質顆粒,通常>70至100μm。 ? ? ? ?除了直接測量聚集體的水平外,還可基于疏水性或蛋白質相互作用對聚集傾向進行排名,因為它們是聚集的主要驅動力。諸如1-苯胺基萘磺酸鹽(ANS)和硫代黃素等熒光染料可用于以最少的樣品需求以高通量方式探測暴露的疏水斑塊。親和捕獲自相互作用納米粒子光譜學(AC-SINS)可提供有關不同溶液條件下的相互作用和聚集傾向的粗粒度信息,可用于在可開發性評估中發揮作用。 ? ? ? ?8. 電荷變異體 ? ? ? ?mAb的電荷變化反映了各種PTM的總和。在整個開發過程中都需要密切監測mAb的變體,以確保一致的峰分布。由于電荷變化對工藝改變的過程非常敏感,因此當工藝發生變化時,電荷變化是證明可比性的具有挑戰性的質量屬性之一。 ? ? ? ?典型的mAb電荷變異體特征是通過基于電荷的方法(例如離子交換色譜法和等電聚焦)表征的,通常包含一個主峰以及幾個較小的酸性和堿性峰。導致形成酸性或堿性物質的修飾如表5所示。值得一提的是,幾種修飾可能會影響mAb變異體的色譜分離,從而徹底改變mAb結構。例如,具有較小寡糖的mAb有助于堿性物質的形成,而氧化的Met可能有助于酸性或堿性物質的形成。類似地,重鏈可變域中的不完全形成的二硫鍵也可能有助于酸性或堿性物質的產生。 ? ? ? ?傳統上使用等電聚焦凝膠電泳(IEF)分析mAb電荷變異體。這種半定量勞動密集型方法依靠染料染色進行檢測。它還具有通量低,缺乏自動化和可重復性差的問題。毛細管IEF(cIEF)克服了IEF的大部分限制,并提供了其他優勢,包括高靈敏度,自動化和低樣品消耗。此外,成像的cIEF(icIEF)在分析mAb電荷變異體方面已廣受歡迎,因為整個毛細管成像消除了傳統cIEF使用的麻煩的操作步驟。 ? ? ? ?毛細管區帶電泳(CZE)可根據電荷和流體動力學半徑分離mAb電荷變體。與cIEF相比,此方法可以輕松以較高通量進行平臺化。CZE也可以與質譜儀在線耦合。CZE-MS已用于分析來自胰蛋白酶肽的N-連接聚糖,并分析脫酰胺和異構化位點。單次CE MS運行已證實可確認100%的一級結構并顯示出多個PTM,包括糖基化,N末端Gln環化,脫酰胺和異構化。 ? ? ? ?離子交換色譜(IEX),包括陽離子交換和陰離子交換,已被廣泛用于監測mAb電荷變體。IEX允許收集餾分以進一步表征。當使用pH梯度時,可以分析多個mAb,這意味著建立平臺方法的潛力。強陽離子交換(SCX)色譜與弱陽離子交換色譜相比,具有相對較高的通量。當比較總體電荷分布時,IEF通常在陽離子或陰離子交換色譜法中顯示出可比的結果。但是,由于分離機理的差異,觀察到了不同的曲線。 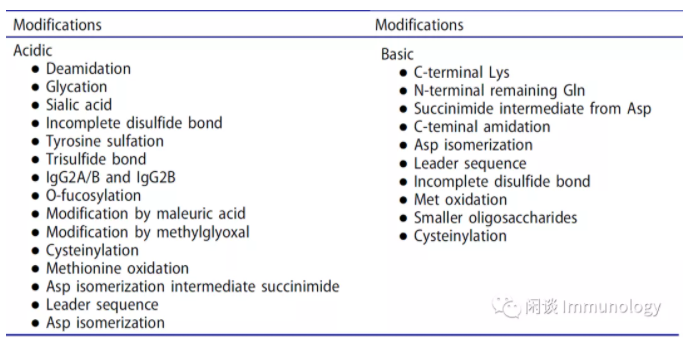
? ? ? ?9. 疏水性和相關異質性 ? ? ? ?疏水性會影響mAb的聚集,溶解度和粘度。較高的疏水性與較高的聚集和沉淀傾向相關。CDR中的疏水性區域可導致更高程度的分子間相互作用,更高的粘度和更短的體內半衰期。 疏水相互作用色譜法(HIC)已用于測量由PTM或降解引起的不同mAb或同一mAb的單獨變體的相對疏水性。與主峰相比,已報告的引起HIC保留時間變化的修飾列于表6中。某些修飾(如Asp異構化和脫酰胺作用)可同時改變HIC保留時間,這表明其他影響色譜行為的因素也參與其中。 ? ? ? ?也有文章報道了用于測量mAb相對疏水性的替代方法,例如通過鹽梯度篩選使用金納米顆粒。在這種方法中,將測試mAb加載到金納米顆粒上,然后施加鹽梯度應力以從mAb分子表面上的疏水斑塊中剝離水分子。結果表明,測試的單克隆抗體與HIC保留時間具有良好的相關性。 ? ? ? ?10. 游離硫醇 ? ? ? ?大量游離Cys的存在會對mAb穩定性和效能產生負面影響。游離Cys和游離Cys相關修飾和降解的水平高度依賴于mAb序列以及細胞培養和純化過程中的環境因素。 單克隆抗體在每個Cys殘基上都含有少量的游離硫醇。游離硫醇可以降低熱穩定性并增加可還原共價聚集體的形成。這些與mAb相關的游離半胱氨酸可與細胞培養基中存在的游離半胱氨酸反應,形成半胱氨酸化或其他共價加合物。在少數情況下,檢測到相對較高的游離半胱氨酸水平,這主要是由于重鏈可變域二硫鍵的形成不完全,導致效能降低。 ? ? ? ?11. 蛋白質-蛋白質相互作用 ? ? ? ?由于蛋白質-蛋白質相互作用對溶解度,粘度和聚集傾向的影響,因此蛋白質-蛋白質相互作用在可開發評估期間引起了越來越多的關注。另外,體內非特異性脫靶結合導致快速清除和不良PK。 ? ? ? ?已開發出多種技術來研究mAb的蛋白質-蛋白質相互作用,包括自身相互作用和與其他分子的非特異性相互作用。在這些技術中,Biacore,生物層干涉法(BLI)和自相互作用納米粒子光譜(SINS)已用于研究自相互作用。另一方面,當固定了不同的蛋白質時,交叉相互作用色譜法(CIC)可用于研究非特異性相互作用。CIC和HIC之間延遲保留之間的正相關關系表明,疏水相互作用是這些mAb總體粘性(非特異性相互作用)的主要促成因素。其他測定法,包括多特異性試劑結合測定法,以及與肝素,HEK293細胞,桿狀病毒顆粒,伴侶蛋白和酵母菌的結合,也已用于研究非特異性相互作用。 ? ? ? ?如涉及知識產權請與我司聯系
主要參考文獻 Mo J, Yan Q, So CK, Soden T, Lewis MJ, Hu P. Understanding the Impact of Methionine Oxidation on the Biological Functions of IgG1 Antibodies Using Hydrogen/Deuterium Exchange Mass Spectrometry.Anal Chem 2016; 88:9495-502.
Yan Y, Wei H, Fu Y, Jusuf S, Zeng M, Ludwig R, et al. Isomerization and Oxidation in the Complementarity-Determining Regions of a Monoclonal Antibody: A Study of the Modification-Structure-Function Correlations by Hydrogen-Deuterium Exchange Mass Spectrometry. Anal Chem 2016;88:2041-50.
Yingda Xu et al,Structure, heterogeneity and developability assessment of therapeutic antibodies,mAbs,2018
Gadgil HS, Bondarenko PV, Pipes GD, Dillon TM, Banks D, Abel J, et al. Identification of cysteinylation of a free cysteine in the Fab region of a recombinant monoclonal IgG1 antibody using Lys-C limited proteolysis coupled with LC/MS analysis. Anal Biochem 2006; 355:165-74. |