? ? ? ?來源:藥學速覽 ▉ 寫在前面 ? ? ? ?分子靶向治療,是在細胞分子水平上,針對已經明確的致癌位點(該位點可以是腫瘤細胞內部的一個蛋白分子,也可以是一個基因片段),來設計相應的治療藥物,藥物進入體內會特異地選擇致癌位點來相結合發生作用,使腫瘤細胞特異性死亡,相比較傳統的化療藥物,靶向藥物不會波及正常組織細胞,所以分子靶向治療又被稱為“生物導彈”。自第一個靶向藥格列衛(伊馬替尼)取得巨大成功以來,靶向癌癥靶點的藥物已經玲瑯滿目,一些癌癥的治療取得了巨大成效,給患者帶來了福音以及希望。 
? ? ? ?但是道高一尺,魔高一丈。狡猾的癌細胞豈能是任人刀俎的魚肉。產生耐藥性是它們抗爭的最直接的表現。比如非小細胞肺癌的治療,由于癌細胞的靶點產生耐藥突變,不得不使靶向藥物升級換代,目前為止已經經歷了三代藥物的更迭(下圖),不幸的是,第三代針對T790M突變藥物奧希替尼也產生了突變,目前面臨沒有新的靶向藥物更換的尷尬局面。再比如費城染色體易位的慢性骨髓性白血病,在經歷第一代靶向神藥格列衛突變后,第二代,第三代的藥物應用而生,比如尼洛替尼,氟馬替尼等。 ? ? ? ?其實除了靶點突變的耐藥機制以外,癌細胞進化出了各種神奇的耐藥機制。比如表達排出藥物的泵系統,俗稱吃了吐。還有會進化出減毒的機制,讓毒性的藥物變成無毒的藥物,以及改變了自身的繁殖方式等等都會產生對當前藥物的抵抗性。最近一篇Science文章指出腫瘤在進行化療時會累積DNA損傷,并會增加基因突變的概率,最終少部分腫瘤細胞會被篩選出來從而進化出各種耐藥性。 ? ? ? ?當癌癥靶向藥物遭遇耐藥后,科學家也并不是束手無策,病人也更不會束手就擒,針對耐藥性本篇文章總結了常見五種針對耐藥性的策略(下圖)。下面將一一進行解讀。 ▉ 設計具有獨特結合模式的抑制劑(1) 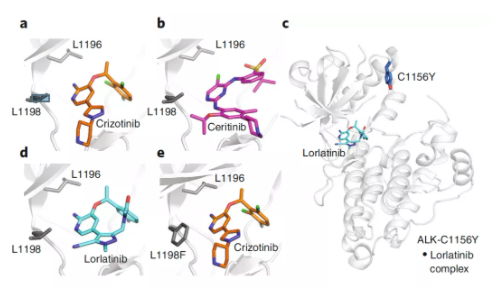
? ? ? ? ALK陽性的肺癌患者治療要首選靶向藥,也就是ALK激酶抑制劑。2011年,克唑替尼(Crizotinib)成為第一個ALK抑制劑,獲得FDA批準用于ALK陽性的NSCLC的一線治療,也問世中國臨床多年。雖然有效,但許多患者在治療約1年后通常會發生耐藥(L1196M)。針對該突變,研發出第二代的藥物,2017年FDA批準了能夠替代克唑替尼的ALK抑制劑-色瑞替尼(ceritinib)。但后續由于檢測到ALK基因繼發突變(C1156Y),該突變提示對第二代靶向藥ceritinib不敏感,但卻是第三代靶向藥lorlatinib的有效靶點。Lorlatinib治療持續8個月有效后,癌癥復發,基因檢測發現,不僅有ALK C1156Y突變,還出現了新的ALK L1198F突變。但是有意思的是,L1198F突變會介導產生lorlatinib耐藥,但卻可以增強第一代ALK靶向藥crizotinib的作用,這種增效作用足以勝過原有的C1156Y突變相關耐藥。所以,患者又從第三代lorlatinib及時換回到第一代crizotinib治療,收獲了較好的效果。 ? ? ? ?著名醫學雜志《New England Journal of Medicine》刊登了這個經典的案例,所以在全程ALK靶向藥治療中,一旦發生耐藥則基于耐藥基因實時監測指導下,從第一代吃到第三代,再換回吃第一代,通過輪換靶向藥成功克服了耐藥。 ▉ 設計共價結合模式的抑制劑(2) ? ? ? ?過去十年里,NSCLC (非小細胞肺癌)治療方案中最顯著的改變可能就是 EGFR 酪氨酸激酶抑制劑用于具有 EGFR 靶向性驅動突變患者一線治療。其中設計開發的共價抑制劑是一大亮點和突破。以EGFR為靶標的第一代非共價抑制劑,如吉非替尼, 厄洛替尼。對治療EGFR~(L858R)突變的NSCLC患者有良好的療效。然而,在接受EGFR抑制劑治療8-14個月后,約60%的患者發生了T790M突變并產生耐藥性。 ? ? ? ?以前大部分的抑制劑是可逆的,科學家腦洞大開,是否可以利用激酶中具有親核功能的基團比如巰基,設計含有親電基團的共價抑制劑呢?于是第二代共價EGFR抑制劑橫空出世,如阿法替尼和達克替尼,被開發用于治療EGFR~(L858R)突變和T790M耐藥突變的NSCLC患者。但這些抑制劑對EGFR~(T790M)突變型和野生型EGFR激酶之間缺乏選擇性 ,因而會產生較強的毒副作用。2018年,FDA批準了第三代共價EGFR抑制劑,如奧希替尼(泰瑞沙),對EGFR~(WT)活性較弱,而對EGFR~(T790M)具有較高的活性及選擇性,減輕了毒副作用。然而,接受其治療的三分之一患者出現了C797S突變并產生耐藥性,也就是把能夠發生共價反應的巰基突變成了羥基(就不讓你反應)。目前針對該突變尚未有合適的靶向藥,如果產生耐藥了,患者可能就要考慮傳統的化療藥物。 ▉ 設計變構結合模式的抑制劑(3) ? ? ? ?變構效應長期以來都被應用于調節正構效應難以靶向的藥物靶標,近年來,它被逐步應用到蛋白相互作用的調節當中。通過變構效應調節蛋白相互作用已經成為創新藥物研發領域的熱點。變構劑保守性低于ATP結合位點,選擇性高,并具有額外的有利性質。當靶點具有雙重結合位點(活性位點和變構位點)時,在單獨給藥產生耐藥突變后,可選擇另外一個位點的靶向藥物,如上圖a,b.? 如果靶向兩個結合位點會怎么樣呢?上圖c所示,雙重抑制(雞尾酒療法)會不會產生1+1>2的效果,會不會克服耐藥性的產生呢? ? ? ? ?最近有研究,在慢性粒細胞白血病(CML)的治療中采用一種新的ABL1激酶變構抑制劑ABL001可以和第二代TKI類藥物尼羅替尼聯用,在小鼠模型中可以起到根治CML的效果。與靶向作用于ATP結合位點的TKI類藥物不同,ABL001作用于正常ABL1蛋白起自我抑制作用的N端豆蔻酰化的帽子結構(MC)的作用位點,從而起到變構抑制激酶活性的作用。有資料顯示,單用ABL001已經可以取得比伊馬替尼(格列衛)更好的效果。但可能更好的信息是相比較使用任意一種藥物產生突變的現象,聯合這兩種藥物的抗突變的能力較強,產生突變的概率更低。 ▉ 設計雙價結合模式的抑制劑(4) mTOR是人類癌癥中都很活躍的細胞信號通路,科學家們已經發展了以天然產物雷帕霉素的類似物第一代藥物比如:依維莫司和西羅莫司等藥物來抑制這條通路。這些藥物靶向mTOR上的雷帕霉素結合位點(FRB)。但是不幸的是大多會產生耐藥突變,比如A2034V以及F2108L突變。針對該突變,開發了第二代mTOR抑制劑,比如AZD8055,MLN0128。它們是通過靶向另一個三磷酸腺苷(ATP)活性位點發揮功能。一些第二代抑制劑已經進入到臨床試驗階段。不幸的是,癌細胞依然會產生耐藥性,第二代mTOR抑制劑也難逃失效的命運。 ? ? ? ?之前研究者發現mTOR上的兩個結合位點相距不過15?。因此他們用一個長度合適的聚乙二醇連接分子將第一代抑制劑雷帕霉素和第二代抑制劑MLN0128連接到一起(上圖)。新分子能夠跨越兩個結合位點,同時與它們結合。這就是第三代mTOR抑制劑,RapaLink-1。它比已有的抑制劑更加強大,而且產生耐藥性的可能性更小。但是這也僅僅在小鼠模型中得到驗證,真正像這種二價的化合物上臨床以及真正成藥還是有難度的。 ▉ 依據蛋白酶體降解策略(5) ? ? ? ?PROTAC 技術通過利用人體自身的泛素-蛋白酶體系統,實現對靶向特定靶點蛋白的降解,只需要小分子藥物短暫地與特定的蛋白結合、給蛋白打上 “泛素化” 的標簽,就可以實現高效特異性的蛋白降解。這種技術在理論上可以靶向大量一直以來被認為 “不可成藥” 的以及容易產生耐藥突變的靶點。不怕你突變,我直接把你滅亡。當然靶點也會在后期重新表達出來,產生不可預知的耐藥。而且PROTACs分子量一般在700~1200之間,透膜能力與口服生物利用度較差,且缺少如適用于小分子藥物的“類藥五原則”的預測模型。但是該策略是克服耐藥性的一個重要的、有意義的應用方向。 ? ? ? ?跟該機理類似的還有“分子膠水”的策略,它也是利用泛素-蛋白酶體系統,能夠介導蛋白質-蛋白質相互作用的小分子化合物。廣義上的分子膠水包括PROTAC。與PROTAC相比,分子膠水具有更小的分子量也更像目前常用的小分子藥物,但是分子膠水的發現也更具有偶然性。 ▉ 總結 ? ? ? ?腫瘤耐藥性問題現在越來越普遍,針對靶點的突變,研究者已經開發了各式各樣的策略應對,很多取得了非常明顯的效果。但是需要注意的是突變是不會停止的,藥物創新也是永恒的話題,盡管創新的道路上荊棘叢生,但是我們一直在路上。 ? ? ? ?如涉及知識產權請與我司聯系
參考出處: https://www.nature.com/articles/s41589-020-0596-8 Cree and Charlton BMCCancer (2017) 17:10 https://science.sciencemag.org/content/368/6495/1127 圖片來源:google,bing,pixabay 注:文章無商業用途,僅用來傳遞知識,如有版權問題,聯系公眾號刪除。 |