? ? ? ?來源:藥學速覽 ? ? ? ?生存的進化壓力推動了耐藥性的出現(xiàn),從而對現(xiàn)代醫(yī)學提出了重大挑戰(zhàn)。耐藥性降低了藥物的有效時間,并限制了患者的治療選擇,在腫瘤學和傳染病的領域中發(fā)生藥物耐藥的機率很高。耐藥性的出現(xiàn)威脅著數(shù)百萬人的生命,并造成了沉重的經(jīng)濟負擔,這促使人們制定新的策略來避免耐藥性。越來越多的藥物被發(fā)現(xiàn)出現(xiàn)耐藥,耐藥產(chǎn)生的機制有很多(圖1),在分子水平上,抗性通常與遺傳變化有關,例如位點突變,缺失和基因擴增,降低耐藥性的機制包括降低有效藥物濃度或消除生存對靶標活性的依賴性等。從歷史上看,耐藥性最初是在治療HIV-1感染時發(fā)現(xiàn)的,在90年代末期,通過聯(lián)合治療直接作用抗病毒的多個靶點。藥物耐藥涉及到了許多領域,包括結構生物學,藥物化學,酶學,計算化學,納米技術,系統(tǒng)生物學等等,都可以用來鑒定耐藥性機制和篩選候選化合物。 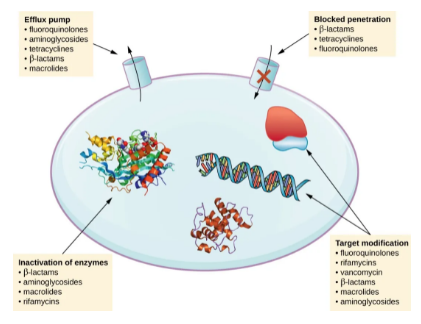
圖 1:耐藥機制 courses.lumenlearning ? ? ? ?Schiffer和他的同事以及Sarafianos和他的同事對病毒的結構,病毒進化和病毒酶的構象動力學有深刻的見解。他們詳細介紹了抗病耐藥的分子機制以及如何應對耐藥的策略。這些策略包含很多方面,例如將抑制劑限制在底物包膜內(nèi),以及與目標蛋白的進化保守特征(活性位點,主鏈原子,金屬配位殘基或變構位點)建立相互作用,這些抑制劑可以與這些蛋白進行結合以避免產(chǎn)生耐藥(圖2)。這樣的基于結構的策略原則上可推廣到所有疾病靶標,抗病毒,抗微生物或腫瘤學。 詳細文章參照:https://pubs.acs.org/doi/abs/10.1021/acs.chemrev.0c00648 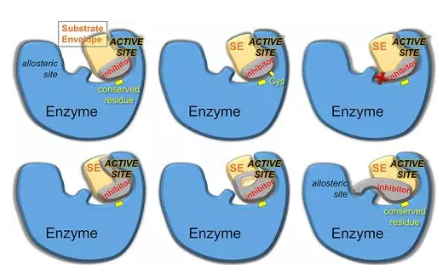
圖2:抗病耐藥的分子機制以及如何應對耐藥的策略?Chemical Reviews ? ? ? ?Paul D. Smith和他的同事強調(diào)了小分子癌癥治療方法中耐藥性的挑戰(zhàn),回顧了19種治療靶標,其中70多種藥物通常采用基于結構的策略進行優(yōu)化。他們描述了為抵抗耐藥性所采取的方法,包括效能和選擇性的提高,作用機理的改變(共價鍵,PROTAC),血腦屏障通透性(BBBP)的提高以及變構口袋的靶向。最后,涵蓋了更廣泛的方法,例如單克隆抗體(mAb),雙特異性抗體,抗體藥物偶聯(lián)物(ADC)和組合療法(圖3)。 詳細文章參照:https://pubs.acs.org/doi/10.1021/acs.chemrev.0c00383 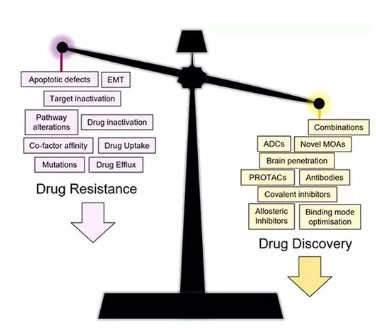
圖3:耐藥機制與藥物發(fā)現(xiàn)?Chemical Reviews ? ? ? ?Aaron Goldman及其同事通過新穎的生物醫(yī)學工程技術來克服腫瘤學中的耐藥性。這些范圍從數(shù)學模型到模擬抵抗發(fā)生的基本進化原理。利用微流控技術測試各種治療策略的生物工程抗藥性腫瘤模型,包括聯(lián)合治療,這些模型成為有效的診斷方法;以及涉及納米技術以增強選擇性藥物輸送以避免耐藥性的療法(圖4)。 詳細文章參照:https://pubs.acs.org/doi/10.1021/acs.chemrev.0c00356 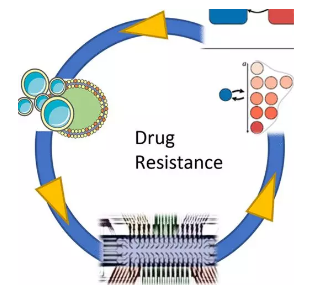
圖4:醫(yī)學工程應對癌癥耐藥性挑戰(zhàn)?Chemical Reviews ? ? ? ?數(shù)十年來,使用β-內(nèi)酰胺類抗生素(如青霉素和頭孢菌素)已成功地成功控制了金黃色葡萄球菌感染。在過去的幾十年中,金黃色葡萄球菌完善了對這些抗生素的耐藥機制,隨后又被新一代的β-內(nèi)酰胺結構所抵消。Jed F. Fisher通過更好地了解金黃色葡萄球菌如何保護β-內(nèi)酰胺酶(青霉素結合蛋白)的酶靶點,探討了當前生物化學和微生物學努力在保護β-內(nèi)酰胺抗生素的未來方面的廣泛性。青霉素結合蛋白是細胞壁生物合成所必需的酶催化劑,了解該細胞壁如何整合到細菌的保護性細胞包膜中可能會鑒定出能保持β-內(nèi)酰胺功效的新抗菌劑和新佐劑(圖5)。 詳細文章參照:https://pubs.acs.org/doi/10.1021/acs.chemrev.0c01010 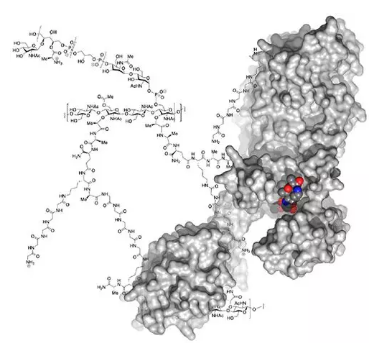
圖5:探索β-內(nèi)酰胺酶的靶點加速針對抗耐藥藥物的研究?Chemical Reviews ? ? ? Gerard D. Wright及其同事通過抗生素耐藥組或賦予耐藥性的所有遺傳成分的集合來觀察抗生素抗藥性。他們著眼于兩類抗生素,氨基糖苷類和四環(huán)素類,并描述了對每類抗生素產(chǎn)生耐藥性的機制。通過這種系統(tǒng)方法,可以了解外排泵,修飾酶和目標修飾物如何改變抗生素的功效。這些機制不僅允許細菌破壞治療手段,而且還是細菌相互競爭并相互保護的機制。他們提出了利用細菌合成機制的抗藥性指導的抗生素發(fā)現(xiàn)模型(圖6)。 詳細文章參照:https://pubs.acs.org/doi/10.1021/acs.chemrev.0c01214 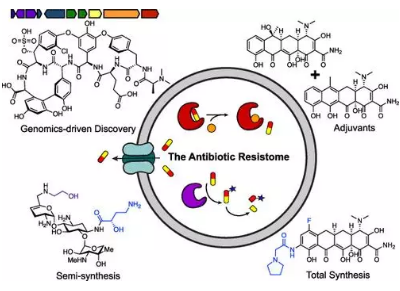
圖6:?天然產(chǎn)物作為抗菌劑的發(fā)現(xiàn)指南?Chemical Reviews ? ? ? ?總的來說,在抗藥性方面,我們需要了解在分子水平上發(fā)生了什么,即進化如何在藥物壓力下實現(xiàn)生存。通過了解進化的約束條件,我們可以利用酶的這些要求來發(fā)揮其強大的抑制劑設計,真菌,細菌和植物用來避免彼此的毒力的策略,以及我們自身的宿主因子參與感染或感染的生長。在醫(yī)學上,次優(yōu)的藥物可能是驅(qū)動耐藥的壓力源。但是,即使使用最好的藥物,我們也可能無法完全避免耐藥性。因此我們需要一種綜合的方法來盡可能地抑制耐藥。通過對化學和生物實體及其對我們自己的微生物組,病毒體和代謝組學的影響的綜合理解,我們可以幫助增強先天性和適應性免疫系統(tǒng),以補充藥物以降低耐藥的可能性。 ? ? ??如涉及知識產(chǎn)權請與我司聯(lián)系
|